작가:
Randy Alexander
창조 날짜:
25 4 월 2021
업데이트 날짜:
26 6 월 2024

콘텐츠
화학에서 용해도는 불용성 잔류 물을 남기지 않고 액체에 완전히 용해되었을 때 고체 화합물의 특성을 설명하는 데 사용됩니다. 이온 화합물 (전하) 만 용해됩니다. 사실, 당신은 단지 몇 가지 원리를 외우거나 문헌을 찾아보기 만하면 이온 화합물이 물에 첨가 될 때 고체 상태로 남아 있는지 또는 많은 양이 용해되는지 알 수 있습니다. 사실, 변화가 보이지 않더라도 일정량의 분자가 용해되므로 정확한 실험을 위해서는이 양의 용질을 계산하는 방법을 알아야합니다.
단계
2 가지 방법 중 1 : 빠른 규칙 사용
이온 화합물에 대해 알아보십시오. 각 원자는 일반적으로 특정 수의 전자를 가지고 있지만 때로는 전자를 얻거나 제공합니다. 이 과정은 하나가됩니다 이온 청구되었습니다. 음전하를 띠는 이온 (전자 1 개 초과)이 양전하 (전자가 없음)를 가진 이온과 만나면 두 자석의 음극과 양극처럼 서로 결합합니다. 결과는 이온 화합물을 형성합니다.
- 이온에는 다음과 같은 음전하가 있습니다. 음이온, 이온은 양이온.
- 일반적으로 원자의 전자 수는 양성자의 수와 같으므로 전하가 없습니다.
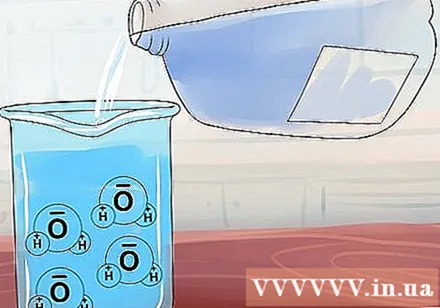
용해도 이해하기. 물 분자 (H2O) 불규칙한 구조를 가지므로 자석과 비슷합니다. 한쪽 끝은 양전하를 띠고 다른 쪽 끝은 음전하를 띠고 있습니다. 이온 화합물을 물에 넣으면 물 "자석"이 그 주위에 모여 양이온과 음이온을 분리하려고합니다.- 일부 이온 화합물은 매우 단단히 흡수되지 않으며 녹는 물에 첨가하면 분리되고 용해되기 때문입니다. 다른 화합물은 더 강한 결합을 가지고 있습니다. 불용성 이온은 물 분자의 인력에 관계없이 서로 단단히 끌어 당겨지기 때문입니다.
- 일부 화합물은 물 분자의 인력과 동등한 결합력을 가지고 있습니다. 그들은 고려됩니다 약간 용해 대부분의 화합물은 분리되지만 나머지는 여전히 서로에게 끌리기 때문입니다.
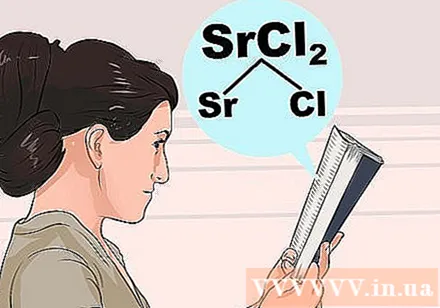
해산의 원리를 이해하십시오. 원자 사이의 상호 작용이 너무 복잡하기 때문에 어떤 화합물이 할 수 있는지 구별하기 위해 전적으로 직관에 의존 할 수 없습니다. 아래 목록에있는 화합물의 첫 번째 이온에서 공통 속성을 찾은 다음 예외를 확인하여 두 번째 이온이 비정상적으로 상호 작용하지 않는지 확인하십시오.- 예를 들어 염화 스트론튬 (SrCl2), 아래의 굵은 단계에서 Sr 또는 Cl을 찾으십시오. Cl은 "보통 가용성"이므로 그 아래의 예외를 확인하십시오. Sr이 예외 목록에 없으므로 SrCl2 가용성이어야합니다.
- 각 규칙에 대한 가장 일반적인 예외는 규칙 아래에 설명되어 있습니다. 다른 예외가 있지만 일반적인 화학 또는 실험실 시간에는 발생하지 않을 수 있습니다.
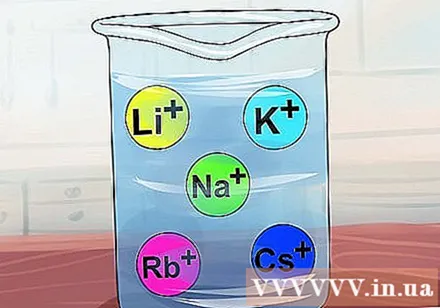
화합물은 Li, Na, K, Rb 및 Cs와 같은 알칼리 금속을 포함 할 때 용해됩니다. 이 금속은 리튬, 나트륨, 칼륨, 루비듐 및 세슘과 같은 IA 족 원소로도 알려져 있습니다. 이러한 이온 중 하나를 포함하는 거의 모든 화합물은 가용성입니다.- 예외: 리3PO4 굳은.
화합물 없음3, 씨2H3영형2, 아니2, ClO3 및 ClO4 모두 용해됩니다. 위의 이온에 해당하는 이름은 질산염, 아세트산 염, 아질산염, 염소산염 및 과염소산 염입니다. 아세테이트는 종종 OAc로 축약됩니다.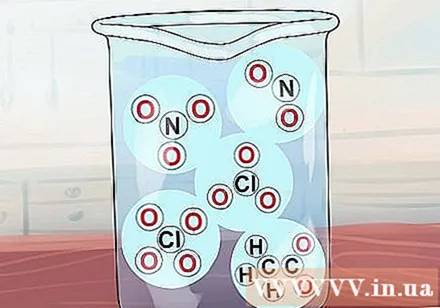
- 예외: Ag (OAc) (은 아세테이트) 및 Hg (OAc)2 (수은 아세테이트) 불용성.
- AgNO2 및 KClO4 단지 "약간 녹아".
Cl, Br 및 I의 화합물은 일반적으로 용해됩니다. 염화물, 브롬화물 및 요오드화물 이온은 거의 항상 할로겐 염이라고하는 용해성 화합물을 형성합니다.
- 예외: 위의 이온이은 이온 Ag와 결합하면 수은 Hg2, 또는 납 납은 불용성 화합물을 형성합니다. 구리 Cu 및 thali Tl과 결합 될 때 형성되는 덜 일반적인 화합물에 대해서도 마찬가지입니다.
SO를 포함하는 화합물4 일반적으로 용해됩니다. 황산염 이온은 종종 용해성 화합물을 형성하지만 많은 예외가 있습니다.
- 예외: 황산염 이온은 다음 이온과 함께 불용성 화합물을 형성합니다 : 스트론튬 Sr, 바륨 Ba, 납 Pb,은 Ag, 칼슘 Ca, 라듐 Ra 및은 모나 톰 Ag2. 황산은과 황산 칼슘은 적당히 용해되기 때문에 일부는 약간 용해된다고 생각합니다.
OH 또는 S를 포함하는 물질은 불용성입니다. 이러한 이온의 해당 이름은 수산화물과 황화물입니다.
- 예외: 알칼리 금속 (그룹 I-A)과 용해성 화합물을 형성하는 방법을 기억하십니까? Li, Na, K, Rb 및 Cs는 모두 수산화물 또는 황화물 이온에 용해되는 화합물을 형성합니다. 또한 수산화물은 알칼리 토금속 이온 (그룹 II-A)에 용해되는 염을 형성합니다 : 칼슘 Ca, 스트론튬 Sr 및 바륨 Ba. 참고 : 수산화물과 알칼리 토금속으로 만들어진 화합물은 실제로 함께 결합 된 상태로 남아있는 분자가 상당히 많으므로 때때로 "약간 용해성"으로 간주됩니다.
CO 함유 화합물3 또는 PO4 굳은. 마지막으로 탄산염과 인산염 이온을 확인하면 화합물이 용해되는지 확인할 수 있습니다.
- 예외: 이러한 이온은 Li, Na, K, Rb 및 Cs와 같은 알칼리 금속과 암모늄 이온 NH와 용해되는 화합물을 형성합니다.4.
방법 2/2 : 상수 K에서 용해도 계산sp
용해도 곱 상수 K 찾기sp. 이 상수는 화합물마다 다르므로 교과서 또는 온라인의 그래프에서 찾아보아야합니다. 이 값은 실험적으로 결정되고 그래프마다 크게 다를 수 있으므로 가능한 경우 교과서의 그래프를 사용하는 것이 가장 좋습니다. 달리 지정하지 않는 한 대부분의 플롯은 테스트 온도가 25ºC라고 가정합니다.
- 예를 들어, 공식 PbI로 요오드화 납을 용해한다고 가정 해 보겠습니다.2, 용해도 곱 상수를 씁니다. bilbo.chm.uri.edu의 그래프를 참조하면 상수 7,1 × 10을 사용합니다.
화학 방정식을 작성하십시오. 첫째, 용해되었을 때이 화합물의 이온 분리 패턴을 결정합니다. 그런 다음 K로 방정식을 작성하십시오.sp 한쪽에는 다른쪽에는 성분 이온이 있습니다.
- 예를 들어, PbI 분자2 이온 Pb, I 및 I로 해리됩니다. (모든 화합물은 항상 전기적으로 중성이기 때문에 이온의 전하를 알거나 확인하기 만하면됩니다).
- 방정식 7,1 × 10 =
- 이 방정식은 용해도 상수이며 용해도 차트에서 2 개의 이온을 찾을 수 있습니다. 2 개의 이온이 있으므로 l-은 2 차이어야합니다.
변수를 사용하도록 방정식을 변환합니다. 분자와 이온의 수에 대해 알고있는 정보를 사용하여 정규 대수 방법을 사용하여 방정식을 다시 작성하십시오. x를 용해시킬 화합물의 질량과 동일하게 설정하고 x가 각 이온의 수를 나타내는 방정식을 다시 작성하십시오.
- 이 예에서는 방정식 7,1 × 10 =
- 화합물에 납 이온 (Pb)이 하나만 있기 때문에 용해 된 분자의 수는 자유 납 이온의 수와 같습니다. 따라서 x로 설정할 수 있습니다.
- 각 납 이온에는 두 개의 요오드 이온 (I)이 있으므로 요오드 원자의 수를 2x로 설정합니다.
- 이제 방정식은 7.1 × 10 = (x) (2x)가됩니다.
공통 이온이있는 경우 고려하십시오. 증류수에 화합물을 용해시키는 경우이 단계를 건너 뜁니다. 화합물이 이미 하나 이상의 성분 이온 ( "공통 이온")이있는 용액에 용해되면 화합물의 용해도가 크게 감소합니다. 일반 이온의 효과는 거의 불용성 화합물에서 가장 분명 할 것이며,이 경우 평형 상태의 대부분의 이온은 이전에 용액 상태였던 이온이라고 가정 할 수 있습니다. 방정식을 다시 작성하여 용액에 이미있는 이온의 몰 농도 (리터당 몰 또는 M)를 계산하고이 값을 해당 이온에 사용하는 변수 x로 바꿉니다.
- 예를 들어, 요오드화 납 화합물이 0.2M 염화 납 (PbCl) 용액에 용해 된 경우2) 방정식을 7.1 × 10 = (0.2M + x) (2x)로 다시 작성합니다. 0.2M은 x보다 농도가 높기 때문에 7.1 × 10 = (0.2M) (2x)로 다시 쓸 수 있습니다.
방정식을 풉니 다. x를 구하면 화합물의 용해도를 볼 수 있습니다. 용해도 상수의 정의에서 물 1 리터당 용해 된 화합물의 몰수로 답을 작성해야합니다. 최종 답을 찾기 위해 컴퓨터를 사용해야 할 수도 있습니다.
- 다음 예는 일반적인 이온이없는 증류수에서의 용해도입니다.
- 7.1 × 10 = (x) (2x)
- 7.1 × 10 = (x) (4x)
- 7.1 × 10 = 4 배
- (7,1 × 10) ÷ 4 = x
- x = ∛ ((7,1 × 10) ÷ 4)
- x = 리터당 1,2 x 10 몰이 용해됩니다.. 이것은 매우 작은 질량이므로이 화합물은 거의 불용성입니다.
필요한 것
- 화합물의 용해도 곱 상수 표 (Ksp)
조언
- 용해 된 화합물의 양에 대한 실험 데이터가있는 경우 동일한 방정식을 사용하여 용해도 상수 K를 구할 수 있습니다.sp.
경고
- 이 용어의 정의에 대한 합의는 없지만 화학자들은 대부분의 화합물에 동의합니다. 용해성 및 불용성 분자가 모두 중요한 구성 요소를 구성하는 여러 특수 화합물로, 각각 이러한 화합물에 대한 설명이 다릅니다.
- 일부 오래된 교과서는 NH를 참조4OH는 가용성 화합물입니다. 이것은 사실이 아닙니다. 소량의 NH 이온이 검출되었습니다.4 및 OH 그러나이 두 이온은 화합물로 결합 할 수 없습니다.



