작가:
Helen Garcia
창조 날짜:
21 4 월 2021
업데이트 날짜:
1 칠월 2024

콘텐츠
화학 방정식은 화학 반응을 상징적으로 표현한 것입니다. 이 경우 반응 화합물(시약)은 왼쪽에, 결과 물질(반응 생성물)은 방정식 오른쪽에 기록됩니다. 반응 방향을 나타내는 화살표가 왼쪽에서 오른쪽으로 그 사이에 배치됩니다. 질량 보존 법칙에 따르면 화학 반응이 진행되는 동안 새로운 원자는 나타나지 않거나 오래된 원자는 사라질 수 없으므로 반응물에 있는 원자의 수는 화학 반응 생성물의 원자 수와 같아야 합니다. . 이 기사에서는 다양한 방법을 사용하여 화학 방정식의 균형을 맞추는 방법을 설명합니다.
단계
방법 1/2: 전통적인 방법
 1 화학 반응식을 쓰십시오. 예를 들어 다음 반응을 고려하십시오.
1 화학 반응식을 쓰십시오. 예를 들어 다음 반응을 고려하십시오. - 씨3NS8 + 오2 -> 에2오 + CO2
- 이 반응은 프로판(C3NS8) 산소가 있는 상태에서 물과 이산화탄소(이산화탄소)를 형성합니다.
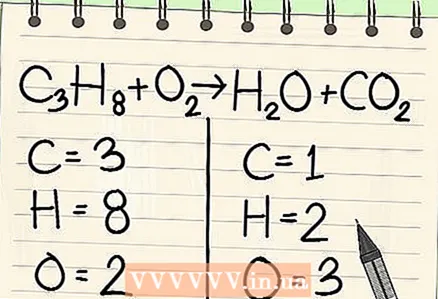 2 각 원소의 원자 수를 기록하십시오. 방정식의 양쪽에 대해 이 작업을 수행합니다. 원자의 총 수를 결정하기 위해 각 원소 옆에 있는 아래 첨자를 참고하십시오. 방정식의 각 원소에 대한 기호를 기록하고 해당 원자의 수를 기록하십시오.
2 각 원소의 원자 수를 기록하십시오. 방정식의 양쪽에 대해 이 작업을 수행합니다. 원자의 총 수를 결정하기 위해 각 원소 옆에 있는 아래 첨자를 참고하십시오. 방정식의 각 원소에 대한 기호를 기록하고 해당 원자의 수를 기록하십시오. - 예를 들어, 고려중인 방정식의 오른쪽에서 추가 결과 3 개의 산소 원자를 얻습니다.
- 왼쪽에는 3개의 탄소 원자(C3), 8개의 수소 원자(H8) 및 2개의 산소 원자(O2).
- 오른쪽에는 1개의 탄소 원자(C), 2개의 수소 원자(H2) 및 3개의 산소 원자(O + O2).
 3 수소와 산소는 왼쪽과 오른쪽에 있는 여러 화합물의 일부이므로 나중을 위해 아껴두십시오. 수소와 산소는 여러 분자의 일부이므로 마지막에 균형을 맞추는 것이 가장 좋습니다.
3 수소와 산소는 왼쪽과 오른쪽에 있는 여러 화합물의 일부이므로 나중을 위해 아껴두십시오. 수소와 산소는 여러 분자의 일부이므로 마지막에 균형을 맞추는 것이 가장 좋습니다. - 수소와 산소의 균형을 맞추기 전에 다른 요소의 균형을 맞추기 위해 추가 요소가 필요할 수 있으므로 원자를 다시 계산해야 합니다.
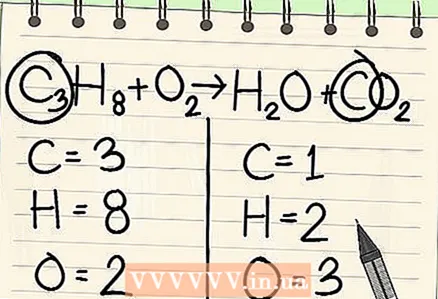 4 빈도가 가장 낮은 항목부터 시작합니다. 여러 요소의 균형을 맞춰야 하는 경우 한 시약 분자와 한 분자의 반응 생성물의 일부인 것을 선택하십시오. 따라서 탄소가 먼저 균형을 이루어야 합니다.
4 빈도가 가장 낮은 항목부터 시작합니다. 여러 요소의 균형을 맞춰야 하는 경우 한 시약 분자와 한 분자의 반응 생성물의 일부인 것을 선택하십시오. 따라서 탄소가 먼저 균형을 이루어야 합니다. 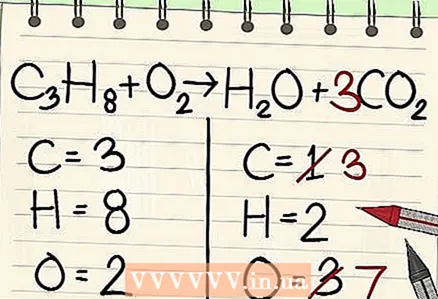 5 균형을 위해 단일 탄소 원자 앞에 요소를 추가합니다. 방정식의 오른쪽에 있는 단일 탄소 앞에 인수를 넣어 왼쪽에 있는 3개의 탄소와 균형을 맞춥니다.
5 균형을 위해 단일 탄소 원자 앞에 요소를 추가합니다. 방정식의 오른쪽에 있는 단일 탄소 앞에 인수를 넣어 왼쪽에 있는 3개의 탄소와 균형을 맞춥니다. - 씨3NS8 + 오2 -> 에2오 + 3CO2
- 방정식의 오른쪽에 있는 탄소 앞에 있는 인수 3은 왼쪽에 있는 프로판 분자의 3개의 탄소 원자에 해당하는 3개의 탄소 원자가 있음을 나타냅니다.
- 화학 방정식에서 원자와 분자 앞에서 계수를 변경할 수 있지만 아래 첨자는 변경되지 않은 상태로 유지되어야 합니다.
 6 그런 다음 수소 원자의 균형을 맞춥니다. 왼쪽과 오른쪽의 탄소 원자 수를 같게 한 후에도 수소와 산소는 불균형 상태를 유지했습니다. 방정식의 왼쪽에는 8개의 수소 원자가 포함되어 있으며 오른쪽에는 같은 수가 있어야 합니다. 비율로 이것을 달성하십시오.
6 그런 다음 수소 원자의 균형을 맞춥니다. 왼쪽과 오른쪽의 탄소 원자 수를 같게 한 후에도 수소와 산소는 불균형 상태를 유지했습니다. 방정식의 왼쪽에는 8개의 수소 원자가 포함되어 있으며 오른쪽에는 같은 수가 있어야 합니다. 비율로 이것을 달성하십시오. - 씨3NS8 + 오2 -> 4시간2오 + 3CO2
- 아래 첨자가 이미 두 개의 수소 원자를 가지고 있음을 보여주기 때문에 오른쪽에 인수 4를 추가했습니다.
- 인수 4에 첨자 2를 곱하면 8이 됩니다.
- 결과적으로 오른쪽에 10개의 산소 원자가 얻어집니다. 3x2 = 3개의 3CO 분자에 있는 6개의 원자2 그리고 4개의 물 분자에 4개의 원자가 더 있습니다.
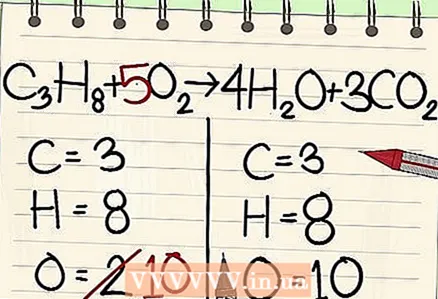 7 산소 원자의 균형을 맞춥니다. 다른 원자의 균형을 맞추는 데 사용한 계수를 고려해야 합니다. 방정식의 오른쪽에 있는 분자 앞에 계수를 추가했기 때문에 산소 원자의 수가 변경되었습니다. 이제 물 분자에는 4개의 산소 원자가 있고 이산화탄소 분자에는 6개의 산소 원자가 있습니다. 따라서 오른쪽에 10개의 산소 원자가 있습니다.
7 산소 원자의 균형을 맞춥니다. 다른 원자의 균형을 맞추는 데 사용한 계수를 고려해야 합니다. 방정식의 오른쪽에 있는 분자 앞에 계수를 추가했기 때문에 산소 원자의 수가 변경되었습니다. 이제 물 분자에는 4개의 산소 원자가 있고 이산화탄소 분자에는 6개의 산소 원자가 있습니다. 따라서 오른쪽에 10개의 산소 원자가 있습니다. - 방정식의 왼쪽에 있는 산소 분자에 인수 5를 추가합니다. 이제 각 조각에는 10개의 산소 원자가 포함됩니다.
- 씨3NS8 + 5시2 -> 4시간2오 + 3CO2.

- 따라서 방정식의 양쪽에는 동일한 수의 탄소, 수소 및 산소 원자가 포함됩니다. 방정식이 균형을 이룹니다.
방법 2/2: 대수적 방법
- 1 반응식을 적으세요. 예를 들어 다음 화학 반응을 고려하십시오.
- PCl5 + H2오 -> H3포4 + 염산
- 2 각 연결 앞에 문자를 넣으십시오.
- NSPCl5 + NSNS2오 -> 씨NS3포4 + NS염산
- 3 방정식의 왼쪽과 오른쪽에 있는 각 원소의 원자 수를 같게 하십시오.
- NSPCl5 + NSNS2오 -> 씨NS3포4 + NS염산
- 왼쪽에 우리는 2NS 수소 원자(각 H에 2개2O), 오른쪽에 있는 동안 3씨+NS 수소 원자 (각 H에 33포4 및 각 HCl 분자에 1개). 왼쪽과 오른쪽이 같은 수의 수소 원자를 포함해야 하므로 2NS 3과 같아야합니다씨+NS.
- 모든 요소에 대해 다음을 수행합니다.
- NS: NS=씨
- 클: 5NS=NS
- H: 2NS=3씨+NS
- 4 계수의 수치 값을 찾기 위해 방정식 시스템을 풉니다. 방정식보다 변수가 더 많기 때문에 시스템에는 여러 솔루션이 있습니다. 모든 계수가 가능한 가장 작은 정수 형태를 갖도록 이러한 솔루션을 찾는 것이 필요합니다.
- 연립방정식을 빠르게 풀려면 변수 중 하나에 숫자 값을 할당하십시오. a = 1이라고 가정합니다. 시스템을 풀고 나머지 변수의 값을 찾습니다.
- P a = c의 경우 c = 1
- Cl 5a = d의 경우, 따라서 d = 5
- H 2b = 3c + d의 경우 값 b를 찾습니다.
- 2b = 3(1) + 5
- 2b = 3 + 5
- 2b = 8
- b = 4
- 따라서 다음 계수가 있습니다.
- 에이 = 1
- b = 4
- c = 1
- d = 5
팁
- 어려움이 있는 경우 온라인 계산기를 사용하여 화학 방정식의 균형을 맞출 수 있습니다. 단, 시험 중에는 이러한 계산기를 사용할 수 없으므로 절대 의존하지 마십시오.
- 때때로 방정식이 단순화될 수 있음을 기억하십시오! 모든 계수가 정수로 나눌 수 있는 경우 방정식을 단순화하십시오.
경고
- 분수 계수를 제거하려면 전체 방정식(왼쪽과 오른쪽)에 분수의 분모를 곱합니다.
- 분수를 화학 방정식의 계수로 사용하지 마십시오. 화학 반응에는 분자나 원자의 반쪽이 없습니다.
- 밸런싱 과정에서 편의상 분수를 사용할 수 있지만 방정식에 분수 계수가 있는 한 방정식은 균형이 맞지 않습니다.