작가:
Bobbie Johnson
창조 날짜:
10 4 월 2021
업데이트 날짜:
1 칠월 2024

콘텐츠
물 분해 과정 (H2O) 전기를 사용하여 구성 요소(수소 및 산소)로 변환하는 것을 전기 분해라고 합니다. 전기 분해의 결과로 얻은 가스는 자체적으로 사용할 수 있습니다. 예를 들어 수소는 가장 깨끗한 에너지 원 중 하나입니다. 이 프로세스의 이름이 다소 영리하게 들릴 수 있지만 올바른 장비, 지식 및 약간의 경험이 있다면 실제로는 보이는 것보다 쉽습니다.
단계
파트 1/2: 장비 준비
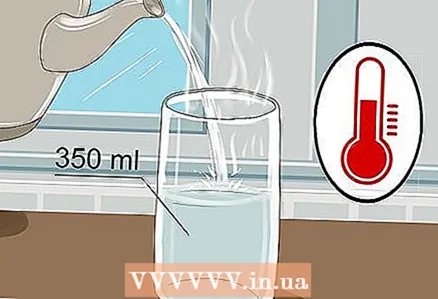 1 350ml 유리잔에 따뜻한 물을 붓습니다. 잔을 가장자리까지 채울 필요는 없으며 약간의 물만 있으면 충분합니다. 따뜻한 물이 전기를 더 잘 전도하지만 찬 물은 할 수 있습니다.
1 350ml 유리잔에 따뜻한 물을 붓습니다. 잔을 가장자리까지 채울 필요는 없으며 약간의 물만 있으면 충분합니다. 따뜻한 물이 전기를 더 잘 전도하지만 찬 물은 할 수 있습니다. - 수돗물과 생수 모두 가능합니다.
- 따뜻한 물은 점도가 낮아 이온이 쉽게 이동할 수 있습니다.
 2 식염 1테이블스푼(20g)을 물에 녹입니다. 유리잔에 소금을 붓고 물을 저어 녹입니다. 이것은 식염수를 생성합니다.
2 식염 1테이블스푼(20g)을 물에 녹입니다. 유리잔에 소금을 붓고 물을 저어 녹입니다. 이것은 식염수를 생성합니다. - 염화나트륨(식염)은 물의 전기 전도도를 증가시키는 전해질입니다. 물 자체는 전기를 잘 전도하지 않습니다.
- 물의 전기 전도도를 높이면 배터리에서 생성된 전류가 용액을 더 쉽게 통과하고 분자를 수소와 산소로 더 효과적으로 분해합니다.
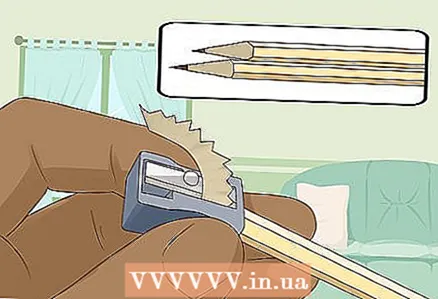 3 두 개의 단단하고 부드러운 연필을 양쪽 끝에서 날카롭게하여 심을 드러내십시오. 연필에서 지우개를 제거하는 것을 잊지 마십시오. 흑연 막대는 양쪽 끝에서 돌출되어야 합니다.
3 두 개의 단단하고 부드러운 연필을 양쪽 끝에서 날카롭게하여 심을 드러내십시오. 연필에서 지우개를 제거하는 것을 잊지 마십시오. 흑연 막대는 양쪽 끝에서 돌출되어야 합니다. - 흑연 막대는 배터리를 연결하는 절연 전극 역할을 합니다.
- 흑연은 물에 녹거나 부식되지 않기 때문에 이 실험에 적합합니다.
 4 유리 위에 놓을 수 있을 만큼 큰 판지를 잘라냅니다. 두 개의 구멍을 뚫은 후에도 처지지 않는 상당히 두꺼운 판지를 사용하십시오. 신발 상자 또는 이와 유사한 것에서 정사각형 조각을 자릅니다.
4 유리 위에 놓을 수 있을 만큼 큰 판지를 잘라냅니다. 두 개의 구멍을 뚫은 후에도 처지지 않는 상당히 두꺼운 판지를 사용하십시오. 신발 상자 또는 이와 유사한 것에서 정사각형 조각을 자릅니다. - 판지는 연필이 유리의 측면과 바닥에 닿지 않도록 물에 연필을 잡는 데 사용됩니다.
- Cardboard는 비전도성이므로 유리 위에 안전하게 올려놓을 수 있습니다.
 5 연필을 사용하여 판지에 두 개의 구멍을 뚫습니다. 연필로 판지를 뚫습니다. 이 경우 단단히 고정되어 미끄러지지 않습니다. 흑연이 유리의 측면이나 바닥에 닿지 않도록 하십시오. 그렇지 않으면 실험을 방해할 수 있습니다.
5 연필을 사용하여 판지에 두 개의 구멍을 뚫습니다. 연필로 판지를 뚫습니다. 이 경우 단단히 고정되어 미끄러지지 않습니다. 흑연이 유리의 측면이나 바닥에 닿지 않도록 하십시오. 그렇지 않으면 실험을 방해할 수 있습니다.
2/2부: 실험 수행
 1 악어 클립이 있는 와이어 하나를 각 배터리 단자에 연결합니다. 배터리는 전류의 소스 역할을 하고 클램프와 흑연 막대가 있는 전선을 통해 전류가 물에 도달합니다.클램프가 있는 와이어 하나를 배터리의 양극에 연결하고 다른 하나는 배터리의 음극 단자에 연결합니다.
1 악어 클립이 있는 와이어 하나를 각 배터리 단자에 연결합니다. 배터리는 전류의 소스 역할을 하고 클램프와 흑연 막대가 있는 전선을 통해 전류가 물에 도달합니다.클램프가 있는 와이어 하나를 배터리의 양극에 연결하고 다른 하나는 배터리의 음극 단자에 연결합니다. - 6볼트 배터리를 사용하세요. 배터리가 없으면 9볼트 배터리를 대신 사용할 수 있습니다.
- 적절한 배터리는 전기용품점이나 슈퍼마켓에서 구입할 수 있습니다.
 2 전선의 다른 쪽 끝을 연필에 연결합니다. 금속 와이어 클램프를 흑연 막대에 단단히 부착합니다. 클립이 흑연 막대에서 미끄러지지 않도록 연필에서 나무를 더 벗겨야 할 수도 있습니다.
2 전선의 다른 쪽 끝을 연필에 연결합니다. 금속 와이어 클램프를 흑연 막대에 단단히 부착합니다. 클립이 흑연 막대에서 미끄러지지 않도록 연필에서 나무를 더 벗겨야 할 수도 있습니다. - 따라서 회로를 닫고 배터리의 전류가 물을 통해 흐릅니다.
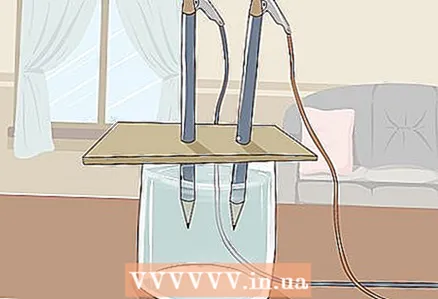 3 연필의 끝이 물에 잠기도록 판지를 유리 위에 놓습니다. 판지는 유리 위에 놓을 수 있을 만큼 커야 합니다. 연필의 올바른 위치를 방해하지 않도록 주의하십시오.
3 연필의 끝이 물에 잠기도록 판지를 유리 위에 놓습니다. 판지는 유리 위에 놓을 수 있을 만큼 커야 합니다. 연필의 올바른 위치를 방해하지 않도록 주의하십시오. - 실험이 성공하려면 흑연이 유리의 벽과 바닥에 닿지 않아야 합니다. 이것을 다시 확인하고 필요한 경우 연필을 조정하십시오.
 4 물이 수소와 산소로 분해되는 것을 지켜보십시오. 물에 잠긴 흑연 막대에서 기포가 올라오기 시작합니다. 이들은 수소와 산소입니다. 수소는 음극에서, 산소는 양극에서 방출됩니다.
4 물이 수소와 산소로 분해되는 것을 지켜보십시오. 물에 잠긴 흑연 막대에서 기포가 올라오기 시작합니다. 이들은 수소와 산소입니다. 수소는 음극에서, 산소는 양극에서 방출됩니다. - 전선을 배터리와 흑연 막대에 연결하자마자 전류가 물을 통해 흐릅니다.
- 각 물 분자는 2개의 수소 원자와 1개의 산소 원자로 구성되어 있기 때문에 음극에 연결된 연필에 더 많은 기포가 형성됩니다.
팁
- 흑연 샤프트가 있는 연필이 없으면 대신 두 개의 작은 와이어를 사용할 수 있습니다. 각 전선의 한쪽 끝을 해당 배터리 극에 감고 다른 쪽 끝을 물에 담그기만 하면 됩니다. 결과는 연필과 동일합니다.
- 다른 배터리를 사용해 보십시오. 흐르는 전류의 양은 배터리의 전압에 따라 달라지며, 이는 차례로 물 분자의 분할 속도에 영향을 미칩니다.
경고
- 소금과 같은 전해질을 물에 첨가하면 실험에서 염소와 같은 소량의 부산물이 생성된다는 점에 유의하십시오. 이러한 소량은 안전하지만 약간의 염소 냄새가 날 수 있습니다.
- 성인 감독하에 이 실험을 수행합니다. 이는 전기 및 가스와 관련이 있으므로 가능성은 낮지만 위험할 수 있습니다.
뭐가 필요하세요
- 단단하고 부드러운 연필 두 개
- 6볼트 또는 9볼트 배터리 1개
- 부피가 350 밀리리터인 유리
- 악어 클립이 있는 2개의 전선
- 연필깎이
- 소금