작가:
Robert Simon
창조 날짜:
24 6 월 2021
업데이트 날짜:
1 칠월 2024

콘텐츠
이론적 수율은 화학 반응에서 기대하는 물질의 최대 양을 화학에서 사용하는 용어입니다. 반응 방정식의 균형을 맞추고 제한 시약을 정의하는 것으로 시작합니다. 사용하고자하는 시약의 양을 측정하면 얻은 물질의 양을 계산할 수 있습니다. 이것은 방정식의 이론적 수율입니다. 실제 실험에서는 이상적인 실험이 아니기 때문에 일부를 잃을 수 있습니다.
단계로
2 단계 중 1 : 제한 시약 결정
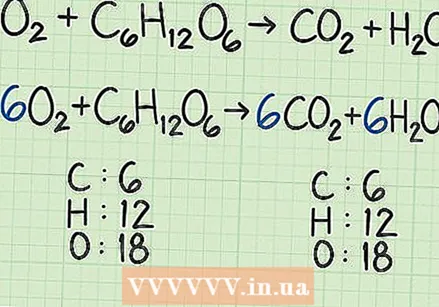 평형 반응으로 시작하십시오. 반응 방정식은 레시피와 유사합니다. 제품을 형성하기 위해 서로 반응하는 시약 (왼쪽)을 보여줍니다 (오른쪽). 평형 반응은 방정식의 왼쪽 (반응물)에 오른쪽 (생성물 형태)과 동일한 수의 원자를 갖습니다.
평형 반응으로 시작하십시오. 반응 방정식은 레시피와 유사합니다. 제품을 형성하기 위해 서로 반응하는 시약 (왼쪽)을 보여줍니다 (오른쪽). 평형 반응은 방정식의 왼쪽 (반응물)에 오른쪽 (생성물 형태)과 동일한 수의 원자를 갖습니다. - 예를 들어, 간단한 방정식이 있다고 가정 해 봅시다.
 각 반응의 몰 질량을 계산하십시오. 주기율표 또는 다른 참고서를 사용하여 각 구성에서 각 원자의 몰 질량을 찾으십시오. 이들을 더하여 각 시약 화합물의 몰 질량을 찾으십시오. 화합물의 단일 분자에 대해 이렇게하십시오. 산소와 포도당을 이산화탄소와 물로 변환하는 방정식을 다시 고려하십시오.
각 반응의 몰 질량을 계산하십시오. 주기율표 또는 다른 참고서를 사용하여 각 구성에서 각 원자의 몰 질량을 찾으십시오. 이들을 더하여 각 시약 화합물의 몰 질량을 찾으십시오. 화합물의 단일 분자에 대해 이렇게하십시오. 산소와 포도당을 이산화탄소와 물로 변환하는 방정식을 다시 고려하십시오. 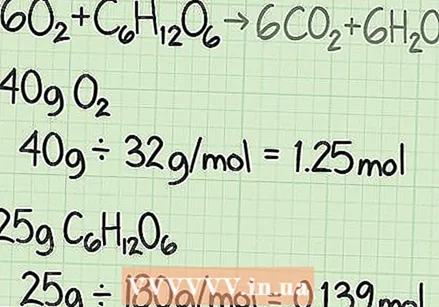 각 시약의 양을 그램에서 몰로 변환합니다. 실제 실험의 경우 사용하는 각 시약의 질량 (g)을 알 수 있습니다. 이 값을 몰 수로 환산하여 해당 물질의 몰 질량으로 나눕니다.
각 시약의 양을 그램에서 몰로 변환합니다. 실제 실험의 경우 사용하는 각 시약의 질량 (g)을 알 수 있습니다. 이 값을 몰 수로 환산하여 해당 물질의 몰 질량으로 나눕니다. - 예를 들어, 40g의 산소와 25g의 포도당으로 시작한다고 가정합니다.
- 40g
 시약의 몰비를 결정하십시오. 몰은 질량을 기준으로 분자를 계산하기 위해 화학에서 사용되는 계산 도구입니다. 산소와 포도당의 몰수를 결정함으로써 각각의 분자 수를 알 수 있습니다. 둘 다의 비율을 찾으려면 한 시약의 몰수를 다른 시약의 몰수로 나눕니다.
시약의 몰비를 결정하십시오. 몰은 질량을 기준으로 분자를 계산하기 위해 화학에서 사용되는 계산 도구입니다. 산소와 포도당의 몰수를 결정함으로써 각각의 분자 수를 알 수 있습니다. 둘 다의 비율을 찾으려면 한 시약의 몰수를 다른 시약의 몰수로 나눕니다. - 다음 예에서는 1.25 몰의 산소와 0.139 몰의 포도당으로 시작합니다. 따라서 산소와 포도당 분자의 비율은 1.25 / 0.139 = 9.0입니다. 이 비율은 포도당보다 9 배 많은 산소 분자를 가지고 있음을 의미합니다.
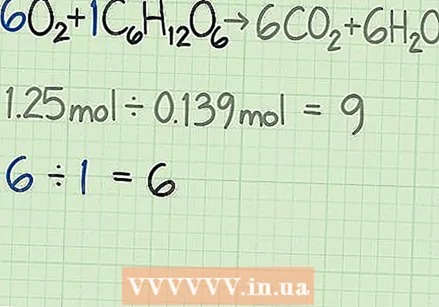 반응에 대한 이상적인 비율을 결정하십시오. 평형 반응을보십시오. 각 분자의 계수는 반응이 발생하는 데 필요한 분자의 비율을 알려줍니다. 공식에 지정된 비율을 정확하게 사용하는 경우 두 시약을 동일하게 사용해야합니다.
반응에 대한 이상적인 비율을 결정하십시오. 평형 반응을보십시오. 각 분자의 계수는 반응이 발생하는 데 필요한 분자의 비율을 알려줍니다. 공식에 지정된 비율을 정확하게 사용하는 경우 두 시약을 동일하게 사용해야합니다. - 이 반응을 위해 반응물은 다음과 같이 주어진다.
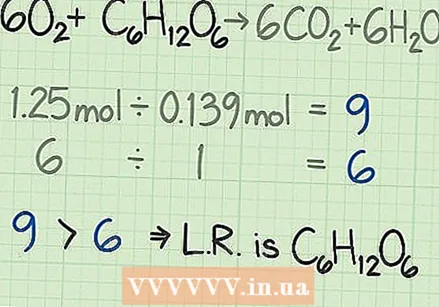 비율을 비교하여 제한 시약을 찾으십시오. 대부분의 화학 반응에서 시약 중 하나는 다른 시약보다 더 빨리 소모됩니다. 먼저 사용되는 시약을 제한 시약이라고합니다. 이 제한 시약은 화학 반응이 지속될 수있는 시간과 예상 할 수있는 이론적 수율을 결정합니다. 계산 한 두 비율을 비교하여 제한 시약을 결정하십시오.
비율을 비교하여 제한 시약을 찾으십시오. 대부분의 화학 반응에서 시약 중 하나는 다른 시약보다 더 빨리 소모됩니다. 먼저 사용되는 시약을 제한 시약이라고합니다. 이 제한 시약은 화학 반응이 지속될 수있는 시간과 예상 할 수있는 이론적 수율을 결정합니다. 계산 한 두 비율을 비교하여 제한 시약을 결정하십시오. - 다음 예에서는 몰로 측정 한 포도당보다 9 배 많은 산소로 시작합니다. 이 공식에 따르면 이상적인 비율은 포도당에 대한 산소의 6 배입니다. 따라서 포도당보다 더 많은 산소가 필요합니다. 따라서 다른 시약,이 경우 포도당은 제한 시약입니다.
- 이 반응을 위해 반응물은 다음과 같이 주어진다.
- 예를 들어, 간단한 방정식이 있다고 가정 해 봅시다.
2/2 부 : 이론적 수율 결정
 원하는 제품을 찾으려면 응답을보십시오. 화학 방정식의 오른쪽은 반응이 생성하는 생성물을 보여줍니다. 반응이 균형을 이루면 각 제품의 계수는 예상 할 수있는 각 분자 비율의 수를 나타냅니다. 각 제품에는 이론적 수율 또는 반응이 완전히 완료되었을 때 예상되는 제품의 양이 있습니다.
원하는 제품을 찾으려면 응답을보십시오. 화학 방정식의 오른쪽은 반응이 생성하는 생성물을 보여줍니다. 반응이 균형을 이루면 각 제품의 계수는 예상 할 수있는 각 분자 비율의 수를 나타냅니다. 각 제품에는 이론적 수율 또는 반응이 완전히 완료되었을 때 예상되는 제품의 양이 있습니다. - 위의 예를 계속하여 응답을 분석합니다.
 제한 시약의 몰 수를 기록하십시오. 제한 시약의 몰수와 제품의 몰수를 항상 비교해야합니다. 각각의 질량을 비교하려고하면 올바른 결과를 얻지 못할 것입니다.
제한 시약의 몰 수를 기록하십시오. 제한 시약의 몰수와 제품의 몰수를 항상 비교해야합니다. 각각의 질량을 비교하려고하면 올바른 결과를 얻지 못할 것입니다. - 위의 예에서 포도당은 제한 시약입니다. 몰 질량 계산에 따르면 처음 25g의 포도당은 0.139 몰의 포도당과 같습니다.
 제품의 분자와 시약의 비율을 비교하십시오. 평형 반응으로 돌아갑니다. 원하는 제품의 분자 수를 제한 시약의 분자 수로 나눕니다.
제품의 분자와 시약의 비율을 비교하십시오. 평형 반응으로 돌아갑니다. 원하는 제품의 분자 수를 제한 시약의 분자 수로 나눕니다. - 이 예의 평형 반응은 다음과 같습니다.
 이 비율에 제한 시약의 몰 수를 곱하십시오. 답은 원하는 제품의 이론적 수율 (몰)입니다.
이 비율에 제한 시약의 몰 수를 곱하십시오. 답은 원하는 제품의 이론적 수율 (몰)입니다. - 이 예에서 포도당 25g은 포도당 0.139 몰과 같습니다. 이산화탄소와 포도당의 비율은 6 : 1입니다. 처음에 포도당의 몰수보다 6 배 많은 이산화탄소를 생산할 수있을 것으로 기대합니다.
- 이산화탄소의 이론적 수율은 (0.139 mol 포도당) x (6 mol 이산화탄소 / mol 포도당) = 0.834 mol 이산화탄소입니다.
 결과를 그램으로 변환하십시오. 이것은 시약의 몰수 또는 양을 계산하는 이전 단계의 반대입니다. 예상 할 수있는 몰의 수를 알고 있으면 여기에 제품의 몰 질량을 곱하여 이론적 수율을 그램 단위로 구하십시오.
결과를 그램으로 변환하십시오. 이것은 시약의 몰수 또는 양을 계산하는 이전 단계의 반대입니다. 예상 할 수있는 몰의 수를 알고 있으면 여기에 제품의 몰 질량을 곱하여 이론적 수율을 그램 단위로 구하십시오. - 다음 예는 CO의 몰 질량입니다.2 약 44g / mol. (탄소의 몰 질량은 ~ 12g / mol이고 산소는 ~ 16g / mol이므로 합계는 12 + 16 + 16 = 44입니다).
- 0.834 몰의 CO 곱하기2 x 44g / mol CO2 = ~ 36.7g. 실험의 이론적 수율은 36.7g의 CO입니다.2.
 원하는 경우 다른 제품에 대해 계산을 반복합니다. 많은 실험에서 특정 제품의 수율에만 관심이있을 수 있습니다. 두 제품의 이론적 수율을 알고 싶다면이 과정을 반복하기 만하면됩니다.
원하는 경우 다른 제품에 대해 계산을 반복합니다. 많은 실험에서 특정 제품의 수율에만 관심이있을 수 있습니다. 두 제품의 이론적 수율을 알고 싶다면이 과정을 반복하기 만하면됩니다. - 이 예에서 물은 두 번째 제품입니다.
. 평형 반응에 따르면 한 분자의 포도당에서 6 분자의 물을 기대할 수 있습니다. 이것은 6 : 1의 비율입니다. 따라서 0.139 몰의 포도당은 0.834 몰의 물이됩니다.
- 물의 몰수에 물의 몰 질량을 곱하십시오. 몰 질량은 2 + 16 = 18g / mol입니다. 제품을 곱하면 0.139 mol H가됩니다.2O x 18g / mol H2O = ~ 2.50 그램. 이 실험에서 물의 이론적 생산량은 2.50g입니다.
- 이 예에서 물은 두 번째 제품입니다.
- 이 예의 평형 반응은 다음과 같습니다.
- 위의 예를 계속하여 응답을 분석합니다.